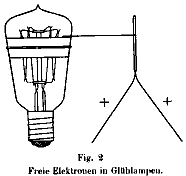
Fig. 2 Freie Elektronen in Glühlampen.
Demonstration of free electrons in an incandescent lamp, detected with an electroscope.
|
Inhalt:
Für das Internet wurden die Teile der Kapitel 3 und 4, sowie das hochspekulative Kap. 10 ausgewählt. |
3. Die Isolierung und Analyse des Elektrons.
Dass wir bei der Ionisierung in Luft gemeinhin die Bausteine nicht
in Freiheit finden, liegt an der Elektronenaffinität des Sauerstoffs.
Um diese zu vermeiden, gibt es aber ausser der Verwendung von Edelgasen
noch ein sehr einfaches Mittel: Man schliesst nach Möglichkeit jedes
Gas aus! Eine eigentliche Ionisierung durch Radium- und Röntgenstrahlen
ist dann zwar nicht möglich; aber durch Licht und Hitze können
wir leicht im Vakuum Elektronen auslösen. Wahrscheinlich ist der verehrte
Leser selbst in der Lage, nach Belieben Elektronen zu erzeugen. Man braucht
ja nur seine elektrische Studierlampe anzudrehen, und schon hat man in
der evakuierten Glühbirne die schönste Elektronenproduktion.
Diese gehen von den leuchtenden Fäden zu Myriaden aus! Aber wie lässt
sich das plausibel machen, wird man mit Recht fragen? Nun wir wollen
ein sehr einfaches Experiment ausführen, das uns wenigstens beweist,
dass Elektrizität vom Glühdraht ins Vakuum übertritt und
zwar fast ausschliesslich nur negative. Wir schneiden uns ein Bändchen
Schokoladenstanniol von einigen Zentimetern Breite und binden den Streifen
mit einem Drähtchen um den Bauch unserer Glühlampe 1) (Fig:2).
Das eine Ende des Drahtes verbinden wir dann mit unserem oben schon vielfach
benützten Elektroskop. Die Lampe soll vorerst nicht brennen. Nun laden
wir das Elektroskop mitsamt dem Stanniolring positiv auf. Das geschieht
direkt mit einer geriebenen Glasstange oder mit dem Hartgummi indirekt
durch Influenz.
Jetzt drehen wir das Licht an. Im selben Moment fallen die Elektroskopblättchen
zusammen! Was ist passiert? Die negativ geladenen Elektronen, die aus dem
Glühdraht kommen, sind gegen den positiv geladenen Stanniolring gestürzt,
allerdings aufgehalten durch die innere Glaswand der Glühbirne. Diese
hat sich negativ aufgeladen und hat durch Influenz fast die ganze positive
Elektrizität auf dem Stanniolring gebunden. Die freie Ladung des Elektroskops
selbst ist daher fast ganz verschwunden. Man kann auch so sagen: Im Anfang
bildet der Stanniolring mit dem Glühfaden einen elektrischen Kondensator
von sehr kleiner Kapazität. Diese steigt nun beim Einschalten der
Lampe gewaltig an, da jetzt die Glaswand innen zur zweiten Belegung wird.
Da aber anderseits die Ladung auf dem Elektroskop unverändert bleibt,
so muss das Potential sinken. Das Elektroskop geht daher auf einen kleineren
Ausschlag zurück.
1) Am besten nimmt man eine noch wenig gebrauchte, d.h. nicht geschwärzte Glühlampe. Hält sich der Elektroskopausschlag infolge schlechter Isolation nicht, so ist die Glühbirne etwas mit Spiritus abzuwaschen.

Fig. 2 Freie Elektronen in Glühlampen.
Demonstration of free electrons in an incandescent lamp, detected with an electroscope.
Nun wollen wir gleich noch feststellen, ob der Glühfaden auch positive
Ionen abgibt. Wir wiederholen das Experiment, mit dem einzigen Unterschied,
dass wir das Elektroskop - aufladen. Wir finden zu unserer Überraschung,
dass beim Einschalten der Glühlampe das Elektroskop nicht muckt! Vielleicht,
dass eine sehr langsame Entladung einsetzt, da infolge unvermeidlicher
Gasreste in der Glühlampe noch eine schwache positive Thermionisierung
vorhanden ist. Diese positive Ionisierung in der Luft ist uns ja durch
ein früheres Experiment bekannt. Wir sehen also den Satz illustriert,
dass auch bei der Thermionisierung die Ablösung von Elektronen das
Primäre ist.
Ähnlich ist es beim lichtelektrischen Effekt, der sich im übrigen.
nicht nur auf die Bestrahlung mit eigentlichem Licht beschränkt. Er
besteht ganz allgemein darin, dass elektromagnetische Wellen Elektronen
aus dem Atom befreien können. Wir haben schon gesehen, dass die kurzwelligen
Strahlen (ultraviolett) besonders wirksam sind. Ganz ebenso erzeugen die
noch viel kürzeren Wellen der Röntgen- und g-Strahlen
des Radiums einen intensiven lichtelektrischen Effekt, hier bekannt unter
der Bezeichnung: Sekundäre Elektronenstrahlung. Also auch hier ist
das Primäre stets die Ablösung von Elektronen. Ihre Austrittsgeschwindigkeit
kann eine ganz beträchtliche sein. Die kinetische Energie der Elektronen
ist nebenbei bemerkt nach dem Einsteinschen Gesetz einfach der reziproken
Wellenlänge des erregenden Lichtes proportional. Relativ kleiner sind
die Austrittsgeschwindigkeiten beim Thermioneneffekt.
Doch wird man vielleicht mit Recht fragen, woher kennt man überhaupt
die Geschwindigkeiten, und wie erkennt man die elektronische Natur der
Partikeln? Wir haben ein einfaches Mittel, um frei bewegte Ionen zu untersuchen.
Erstens sind sie durch elektrische Kräfte beeinflussbar, zweitens
aber ebensosehr durch magnetische. Denn bewegte Ionen repräsentieren
fliessende Elektrizität, und auf solche übt ein Magnet eine mechanische
Kraft aus (Biot-Savartsches Gesetz). Am besten zeigen wir das an einem
Kathodenstrahlrohr, das wir in der Braun-Wehneltschen Ausführung in
Fig. 3 sehen. Wir erzeugen eine elektrische Entladung, indem wir an die
Metallplatte K und den Zylinder A die Spannung eines kleinen Induktoriums
anlegen. Die Luft im Rohr sei soweit verdünnt, dass die von der Platte
K ausgehenden Ionen durch die Luftreste nur wenig gebremst und daher im
elektrischen Felde zwischen K und A stark beschleunigt werden. Sie erlangen
dann eine solche Geschwindigkeit, dass sie durch das zentrale Loch in A
hindurchfliegen und schliesslich auf die Glaswand auftreffen. Den Ionenstrahl
sehen wir durch das Leuchten der von ihm durchsetzten Gasreste; und beim
Aufprallen auf die Glaswand beobachten wir einen intensiv grünen Fluoreszenzfleck.
Einen lebhaft blauen Aufstosspunkt erhält man, wenn vor das Glas ein
Fluoreszenzschirm aus Calciumwolframat gesetzt wird (Fig. 3). Der Strahl
besteht, wie aus der Wahl der Polarität von K zu erwarten ist, aus
negativen Ionen. Man kann dies aber auch leicht feststellen. Ladet man
die eingeschmolzenen Kondensatorplättchen PP' auf eine Spannungsdifferenz
von einigen hundert Volt auf, so biegt sich der Strahl nach dem positiv
geladenen Plättchen hin.
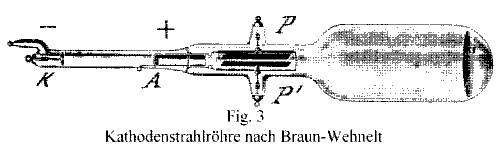
Fig. 3 Kathodenstrahlenröhre nach Braun-Wehnelt.
cathode ray tube
K: cathode; A: ring anode; at the right end a CaWolframate-fluorescent-screen
(with only one deflection pair P P' in vertical direction, the horizontal
deflection was done with a rotating mirror)
Die Ablenkung, die der Leuchtfleck auf dem Fluoreszenzschirm erfährt,
lässt sich zahlenmässig angeben, wenn man die Rohrdimensionen
und die Potentialdifferenz an den Plättchen P P. kennt, unter der
Voraussetzung, dass jedem Ion eine Ladung e, eine Masse m und eine Geschwindigkeit
v zukomme. Ganz ebenso bekommen wir eine Ablenkung des Strahles, wenn wir
einen Hufeisenmagneten heranbringen. Befindet sich etwa der Nordpol unten,
der Südpol oben, so würde der Strahl vorne aus der Zeichnungsebene
heraustreten. Man kann bei definierten Verhältnissen wiederum eine
Beziehung angeben, in der neben den Rohrdimensionen und der Stärke
des Magnetfeldes auch die Grössen e, m und v vorkommen. Diese Grössen
aus zwei Beziehungen zu berechnen, ist natürlich nicht möglich.
Indessen treten in den Formeln e und m nur in der Verbindung e/m auf. Man
hat also eigentlich nur zwei unbekannte Grössen: e/m und v, und diese
lassen sich infolgedessen nach der klassischen Methode der elektrischen
und magnetischen Ablenkung bestimmen. e/m ist die Ladung pro Masseneinheit
oder die spezifische Ionenladung. Sofern man nun annehmen darf, dass die
Ladung e bei allen Ionen die gleiche sei, kann man die Masse verschiedener
Ionen einfach dadurch miteinander vergleichen, dass man e/m für beide
Ionenarten bestimmt. Man kann z. B. im Prinzip an der gleichen Röhre
m (Fig. 3) die Masse positiver und negativer Ionen miteinander vergleichen.
Verbindet man nämlich K mit dem + - und A mit dem - -Pol des Induktors,
so treten aus dem Diaphragma positive Ionenstrahlen, sog. Kanalstrahlen,
aus. Für diese Strahlen hat man gefunden, dass höchstens den
Wert 9650 elektromagnetischer Einheiten pro Gramm haben kann. Dies ist
der Wert, der für das Wasserstoff-Ion der Elektrolyse gilt. Das positive
Ion hat daher stets mindestens eine Masse, die gleich dem des leichtesten
Atoms ist, es sind also Massestrahlen; meist Atome, die ein Elektron verloren
haben. Bei den Kathodenstrahlen aber hat sich ergeben, dass e/m den
hohen Wert 1.77E7 hat. Die negativen Teilchen besitzen daher eine Masse,
die im Verhältnis zum Wasserstoffatom beträgt: 9650/1.77E7 =
1/1830. Dadurch wird es uns aber zur Gewissheit, dass die Elektronen wirklich
subatomaren Charakter haben.
Die Methode der elektrischen und magnetischen Ablenkung lässt
sich auch für lichtelektrische und Thermionen anwenden. In allen Fällen
hat sich gezeigt: elektrische Ladung im Vakuum besteht aus Elektronen.
Ob man Elektronen oder Masse-Ionen vor sich hat, lässt sich meist
schon ohne quantitative Bestimmung entscheiden. Da für Elektronen
die spezifische Ladung e/m sehr gross ist, so ist die Ablenkung bereits
durch kleine magnetische Kräfte ausführbar, im Gegensatz zu den
Massestrahlen, die stets schwer ablenkbar sind.
4. Die Elektronenröhren.
Bevor wir uns weiter mit dem Begriff der Elektronen beschäftigen,
wollen wir der Anschaulichkeit halber erst an einigen Beispielen zeigen,
wie man sich die Eigenschaften der freien Elektronen zunutze gemacht hat.
Eine erste Anwendung erlaubt die oben schon beschriebene BRAUN-WEHNELTsche
Kathodenstrahlröhre. Sie dient zur Untersuchung des zeitlichen Verlaufs
von elektrischen Strömen und Spannungen. Die Ablenkung des Fluoreszenzflecks
erfolgt ja in jedem Moment proportional den ablenkenden elektrischen bezw.
magnetischen Kräften. Sofern diese also zeitlich variieren, wird der
Leuchtpunkt gewisse Kurven beschreiben. Da die Bewegung sozusagen trägheitsfrei
erfolgt, können so selbst die raschen Schwingungen der drahtlosen
Telegraphie ohne Schwierigkeit aufgelöst und analysiert werden. Wir
wollen in Fig. 5 ein Bild für die Spannungsänderung an einem
Kondensator wiedergeben, wenn dieser durch eine Gleichrichteranordnung
mittels Wechselstrom aufgeladen wird.
Die Klemmen des Kondensators wurden bei dem Versuch einfach mit den
Metallplättchen PP' der Braunschen Röhre (Fig.3) verbunden. Man
sieht in Fig. 5a, wie der Leuchtpunkt sich ruckweise aus der Stellung A
in die Stellung B bewegt hat. Wäre er gleichmässig gewandert,
so hätte sich eine leuchtende Linie abbilden müssen. Noch besser
sieht man die Bewegung, wenn man sie im rotierenden Spiegel betrachtet.
Man erhält dann das Bild Fig. 5b. Der Spannungsanstieg erfolgt treppenförmig
vom Wert A zum Wert B, und die Spannung bleibt dann auf der Höhe von
B. Die Reihe von Lichtpunkten unten markieren die Zeitmarken im Abstand
von je 1/100 Sekunde und lassen erkennen, dass die Kondensatorspannung
alle 1/50 Sekunde ruckweise angestiegen ist.
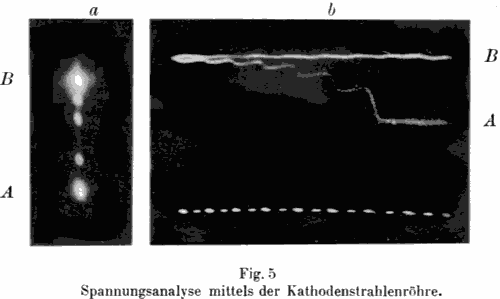
Fig. 5 Spannungsanalyse mittels der Kathodenstrahlenröhre.
Analysis of voltage of a capacitor with a cathode ray tube.
a: ordinary picture
b: picture in a rotating mirror
10. Das positive Elektron.
Doch kehren wir wieder zu unserem Kernproblem zurück. Wir wissen
bereits, der Atomkern ist nicht einfacher Natur. Er ist zum mindesten bei
den radioaktiven Substanzen zusammengesetzt und enthält, wie die radioaktiven
Zerfallsreihen zeigen, eine ganze Anzahl Heliumteilchen. Es erhebt sich
sofort die Frage, lassen sich alle Atomkerne etwa als Aggregate von Heliumkernen
auffassen? Ein Blick auf die Atomgewichte lehrt uns, dass dies nicht möglich
ist. Die Atomgewichte sind nur zum kleinsten Teil Multiple von vier. Wir
müssen also schon noch nach anderen Bausteinen der Atomkerne suchen.
Die nächstliegende Annahme ist die Beteiligung von Wasserstoffkernen
beim Kernaufbau. Jedenfalls lässt sich dann jedes Atomgewicht als
Summe einer Anzahl von Helium und von Wasserstoffkernen darstellen. Hierbei
ist allerdings vorausgesetzt, dass sämtliche Atomgewichte ganzzahlig
sind. Durch die neueren Forschungen des Engländers ASTON über
die Isotopenanalyse dürfen wir dies aber tatsächlich als richtig
annehmen. Zum Glück müssen wir uns aber heute nicht mehr mit
der blossen logischen Möglichkeit vom Wasserstoffaufbau der Kerne
begnügen. Durch die Aufsehen erregenden Untersuchungen von RUTHERFORD
dürfen wir es als Tatsache ansehen, dass Atomkerne Wasserstoff enthalten.
Zunächst gelang der Nachweis, dass das Stickstoffatom Wasserstoff
enthält. Nicht etwa, dass es bis heute gelungen wäre, die Bildung
von Wasserstoff aus Stickstoff chemisch zu erweisen, wohl aber konnte man
den Wasserstoff in Form der oben schon genannten H-Strahlen feststellen.
Wir erinnern daran, dass a-Teilchen beim Aufprall
auf H-Kerne H-Strahlen von einer Reichweite von 29 Zentimetern erzeugen,
während die a-Teilchen von Radium C selbst
nur 7 Zentimeter weit zu fliegen vermögen. Beim Auftreffen auf schwerere
Atomkerne entstehen andererseits Sekundärstrahlen, die eine viel kleinere
Reichweite als die erzeugenden a-Strahlen haben.
Man beachte etwa die kurzen Zacken der Gabelungen in den WILSONschen Nebelbildern
(Fig. 12)!
Immer also, wenn die von den a-Strahlen
gestossenen Partikel eine abnorm grosse Reichweite aufweisen kann man auf
die Existenz von H-Strahlen schliessen. RUTHERFORD beobachtete nun, dass
in reinem Stickstoff Korpuskularstrahlen von 40 Zentimeter Reichweite erzeugt
werden und schloss hieraus, dass aus den Stickstoffkernen H-Kerne herausgeschossen
würden. Im einzelnen wurde dann die Natur der H-Strahlen auch noch
durch deren magnetische und elektrische Ablenkung als solche erkannt. Es
konnte daher kaum noch daran gezweifelt werden, dass die ungeheure Energiekonzentration
der a-Teilchen imstande ist, Atomkerne zu zertrümmern.
Dass durch eine ungeheure Zahl von a-Teilchen
nur sehr wenige H-Strahlen gebildet werden (Verhältnis 1010:1), hängt
damit zusammen, dass die Stickstoffkerne bei ihrer geringen Ausdehnung
(Radius =10-12 Zentimeter) nur selten zentral getroffen werden.
Dies stimmt zwar aufs beste mit den theoretischen Voraussetzungen, lässt
es aber als fast hoffnungslos erscheinen, dass man den künstlichen
atomistischen Zerfall wird chemisch nachweisen können.
Von RUTHERFORD sind in der Folge eine ganze Reihe von Elementen untersucht
worden, und ist das Auftreten von H-Strahlen noch bei Bor, Fluor, Natrium,
Aluminium und Phosphor, alles Elementen vom Atomgewicht kleiner als 32,
festgestellt worden. Die Reichweite der H-Strahlen war sehr verschieden
Sie betrug bei Aluminium sogar 90 Zentimeter! Daraus geht hervor, dass
die Energie der H-Strahlen teilweise aus dem Atomkern selbst stammt und
überdies, je nach dem Element, einen verschiedenen Betrag hat. Durch
die a-Teilchen wird also eine inneratomistische
exotherme Reaktion eingeleitet. Würde jedes a-Teilchen
bezw. jedes erzeugte H-Teilchen zum gänzlichen Zerfall führen,
so könnten wir die gesamte Atomenergie nutzbar machen. Ein einziges
a-Teilchen
würde genügen, um die Atomenergie auszulösen, die Masse
würde wie angezündetes Thermitpulver abbrennen! Selbst wenn die
Katastrophe nur unsere leichteren Elemente beträfe, was würde
dann aus uns und unserer Erde? Das Resultat wäre Wasserstoff und Helium.
Denn, wir müssen annehmen, dass nicht nur die radioaktiven Elemente,
sondern auch die leichten Atomkerne teilweise aus Helium aufgebaut sind.
Ja, die RUTHERFORDschen Versuche führen sogar zum Schluss, dass die
Elemente nur durch 4 teilbarem Atomgewicht ausschliesslich aus Helium bestehen.
Konnten doch weder bei Kohlenstoff (12), noch bei Sauerstoff (16), noch
bei Schwefel (32) H-Strahlen beobachtet werden. Nun liegt die Annahme nahe,
dass auch bei den anderen Elementen der grösste Teil aus Heliumkernen
aufgebaut ist und nur der Rest, soweit das Atomgewicht nicht durch 4 teilbar
ist, aus H-Kernen besteht.
Unsere Kernanalyse führt also zunächst zu zwei Urstoffen.
Es liegt nun die Frage nahe, können wir nicht mit PROUT annehmen,
dass alle Atomkerne letzten Endes aus einem einzigen Stoff aufgebaut und
dass die Heliumkerne also bereits zusammengesetzter Natur sind? Den Heliumkern
als einen Verband von 4 Wasserstoffkernen anzusehen, dem steht nichts entgegen.
Wohl aber wäre dann eine Erklärung erwünscht, warum trotz
der ungeheuren Heftigkeit des radioaktiven Zerfalls nicht H-Kerne sondern
He-Kerne ausgeschleudert werden. Dies kann nur dann möglich sein,
wenn der Heliumkern einen Verband von sehr hoher Stabilität darstellt.
Dass dies tatsächlich der Fall ist, lässt sich ohne genaue Kenntnis
des Heliumkerns natürlich nicht ausrechnen. Es ist aber wiederum der
EINSTEINsche Energiesatz, der uns auch ohne diese Kenntnis den Beweis
in elegantester Weise zu erbringen erlaubt. Das Atomgewicht des Wasserstoffs
ist genau 1,0077, das des Heliums 4,000. Wenn wir uns also Wasserstoffkerne
zu Heliumkernen verarbeitet denken, so entsteht immer aus 1,0077 Gramm
Wasserstoff 1 Gramm Helium. Es tritt dabei also ein Gewichtsverlust von
0,0077 Gramm auf. Dies entspricht aber dem Freiwerden einer Verbindungsenergie
von 0,0077 * c2 Erg. Bilden wir statt 1 Gramm Helium nur ein
einziges Atom vom Gewicht m Gramm, so wäre die entsprechende atomare
Bildungsenergie 0,0077* c2 *m Erg. Das wäre nun aber auch die Energie,
die man zur völligen Zertrümmerung eines Heliumkernes aufwenden
müsste. Nun wollen wir sehen, wie gross dagegen die kinetische Energie
eines a-Teilchens ist. Diese schreiben wir statt
m/2*v2 in der Form m/2*( v/c)2 * c2. Da
z. B. für Radium C v/c= 1/15 ist, so erhält man für die
gesuchte Energie m/2*(1/15)
2 * c2 = 0,0022
*c2*m Erg. Dies ist aber mehr als dreimal zu wenig, um einen
Heliumkern zu sprengen; denn es ist 0,0022/0,0077 = 0,29. Wir verstehen
daher, dass die a-Partikel mit ihrer grossen
Geschwindigkeit aus dem Atomverband herausgeschleudert werden können,
ohne dass sie dabei in die einzelnen H-Kerne auseinanderfliegen.
In analoger Weise können wir nun auch versuchen, die Abweichungen
der Atomgewichte von der Ganzzahligkeit zu erklären. Denn sie können
in sehr einfacher Weise zu der Bildungsenergie der Atome in Beziehung gesetzt
werden. Die Kleinheit der Abweichungen besagt dabei, dass die im Kern aufgespeicherte
Energie, also u. a. die gewaltige radioaktive Energie, noch klein ist im
Verhältnis zur Energie der konstituierenden H-Kerne selbst. Wichtig
ist der Umstand, dass die Ganzzahligkeit der Atomgewichte nur dann herauskommt,
wenn man sie auf Sauerstoff 16, d.h. eben auf Helium 4 bezieht. Das würde
dann die Anschauung bestätigen, dass die Atome zum grössten Teil
aus Heliumkernen aufgebaut sind, und dass die Energie, die beim Zusammenschluss
dieser Heliumkerne und allfälliger H-Kerne zum Atomkern noch frei
wird, relativ klein ist! Wenn nun die eventuell verfügbare Atomenergie,
die bei radioaktiver Umwandlung gewonnen werden kann, so klein zu bemessen
ist, wie geringfügig muss da erst die chemische Energie erscheinen.
Dass da Versuche eines LANDOLT um Massenänderungen bei chemischen
Reaktionen nachzuweisen, negativ ausfallen mussten, scheint uns in diesem
Lichte ganz natürlich. Die Energieumsätze des täglichen
Lebens sind eben Bagatellen im Hinblick auf die ungeheuerlichen in der
Masse schlummernden Arbeitskräfte.
Fragen wir nun nach den Dimensionen der H-Kerne, so gelangen wir zu
einem Ergebnis, das uns durch seine Kleinheit überrascht. Es
hindert uns nichts, für diese Teilchen dieselbe Konstitution wie für
das Elektron anzunehmen. Wir hätten dann kleine Kügelchen vor
uns, auf deren Oberfläche je eine positive Elementarladung verteilt
wäre. Denn, da ein H-Kern und ein Elektron, zu einem neutralen H-Atom
zusammentreten, so kann es sich ja nur um die Einheitsladung handeln. Nun
können wir wieder dieselbe Beziehung (4) wie früher anwenden.
Wir beachten, dass, sowohl für den H-Kern als das Elektron das Produkt
m a denselben Wert geben muss. Da aber m' für den Wasserstoffkern
1830 mal grösser ist als für das Elektron, so heisst das, sein
Radius a muss 1830 mal kleiner sein als dort. D.h. der H-Kern hat einen
Radius von 1,88. 10-13:1830 = 1,03.10-16 Zentimeter.
Er repräsentiert daher einerseits die grösste uns bekannte Energiekonzentration
und andererseits das kleinste Teilchen. Mit seiner Kleinheit zusammen hängt
es auch, dass Berechnungen der auf dem positiven Elektron herrschenden
Spannung und der Dichte der Teilchen noch zu weit extremeren Werten als
beim Elektron führen müssen (siehe S.15). Im übrigen aber
unterscheidet sich der H-Kern vom Elektron nur durch das positive Vorzeichen
der Ladung. Man kann daher von positiven Elektronen reden; und mit Rücksicht
darauf, dass diese zugleich die Urmasse repräsentieren, kann man auch
die Bezeichnung Protonen gelten lassen. Doch das sind Worte. Tatsache
ist, dass wir für den Aufbau der Atome nur zweierlei Bausteine anzunehmen
haben: das positive und das negative Elektron. Unsere Auffassung von der
Elektrizität und damit auch von der Materie ist also eine dualistische,
darin begründet, dass wir die Vorgänge im Atom als das Wechselspiel
anziehender und abstossender Kräfte ansehen müssen.
Bemerkung: Schon bei der Beschreibung des Elektrons wird darauf hingewiesen,
dass die Betrachtung nur dann richtig sei, wenn man sich das Elementarteilchen
aus unendlich vielen, noch kleineren Teilchen zusammengesetzt vorstelle,
und wenn die Gesetze der klassischen Physik anwendbar seien. In dieser
Beschreibung werden Neutronen als "positive Elektronen"=Protonen aufgefasst,
welche ein "Kern-Elektron" enthalten.
Das heutige Standardmodell sieht etwas anders aus.
Die Arbeit enthält auch Bauanleitungen von einem Ultragalvanometer, einer Wilsonschen-Nebelkammer, einem knackenden Geigerzähler und einem Apparat für den Nachweis kurzlebiger Isotope (Halbwertzeit < Minuten).
Der Ausblick auf Seite 31 beschäftigt sich mit der Kernspaltung mit Hilfe von Alfa-Teilchen, dem Ruf nach Beschleunigern und der Kernfusion.